Esperamos que
nuestros lectores hayan tenido unas buenas vacaciones de verano.
Empezamos un
nuevo curso escolar y retomamos uno de los temas favoritos de este blog a la
vista de la frecuencia con la que volvemos sobre él: el precio de los fármacos
y, en particular, de los fármacos para el cáncer .
 Un artículo de reciente aparición en el Journal of Economic Perspectives (Pricing in the Market for Anticancer Drugs) mostraba como los precios de los
principales fármacos para el tratamiento del cáncer habían aumentado muy por
encima de las tasas de inflación en las dos últimas décadas: en 2013 los 58
principales fármacos costaban alrededor de 207.000$ por año de vida ganado,
cuando en 1995 costaban 54.000$. Los autores sugieren que el aumento de los
precios responde a una mayor tolerancia social (disponibilidad a pagar) a unos
costes sanitarios elevados. Los políticos son rápidos en ponerse de acuerdo en
que el sistema de salud debe desalentar el uso de tratamientos ineficaces, pero
no está claro cómo los reguladores, compañías de seguros y médicos deben afrontarse
a tratamientos que son mucho más costosos, pero que ofrecen beneficios
incrementales pequeños.
Un artículo de reciente aparición en el Journal of Economic Perspectives (Pricing in the Market for Anticancer Drugs) mostraba como los precios de los
principales fármacos para el tratamiento del cáncer habían aumentado muy por
encima de las tasas de inflación en las dos últimas décadas: en 2013 los 58
principales fármacos costaban alrededor de 207.000$ por año de vida ganado,
cuando en 1995 costaban 54.000$. Los autores sugieren que el aumento de los
precios responde a una mayor tolerancia social (disponibilidad a pagar) a unos
costes sanitarios elevados. Los políticos son rápidos en ponerse de acuerdo en
que el sistema de salud debe desalentar el uso de tratamientos ineficaces, pero
no está claro cómo los reguladores, compañías de seguros y médicos deben afrontarse
a tratamientos que son mucho más costosos, pero que ofrecen beneficios
incrementales pequeños.
Últimamente han aparecido tres iniciativas encaminadas a iluminar –aunque sea un poco- el
camino. Por un parte las American Society of Clinical Oncology ha diseñado un marco para determinar el
valor de los fármacos para el cáncer en función de su beneficio clínico,
toxicidad, costes y “extras” (paliación de síntomas o tiempo sin tratamiento)
en el que habla explícitamente de AVAC y ratios coste-efectividad
incrementales. De hecho, la ASCO fue una de las sociedades que se unió a la iniciativa
del Choosing Wisely, indicando cinco prácticas que no añadían valor en el tratamiento del cáncer .
De forma
parecida, pero en el continente europeo, la European Society for Medical
Oncology ha diseñado la ESMO Magnitude of Clinical Benefit Scale para evaluación del valor de los fármacos
para el cáncer en función de la supervivencia que ofrecen y su toxicidad. En un
artículo de próxima aparición en Annals of Oncology, el Dr. Tabernero del
Hospital Vall d’Hebron y próximo presidente de la ESMO ha declarado que dejar
de lado el precio de los fármacos no es una opción, y que se tendrá que tener
en cuenta en una próxima versión de la ESMO-MCBS.
Volviendo a
Estados Unidos, los oncólogos del Memorial Sloan-Kettering Cancer Center siguen
su particular batalla contra los elevados precios de los fármacos para el
cáncer, de la que ya se había hecho eco este blog.
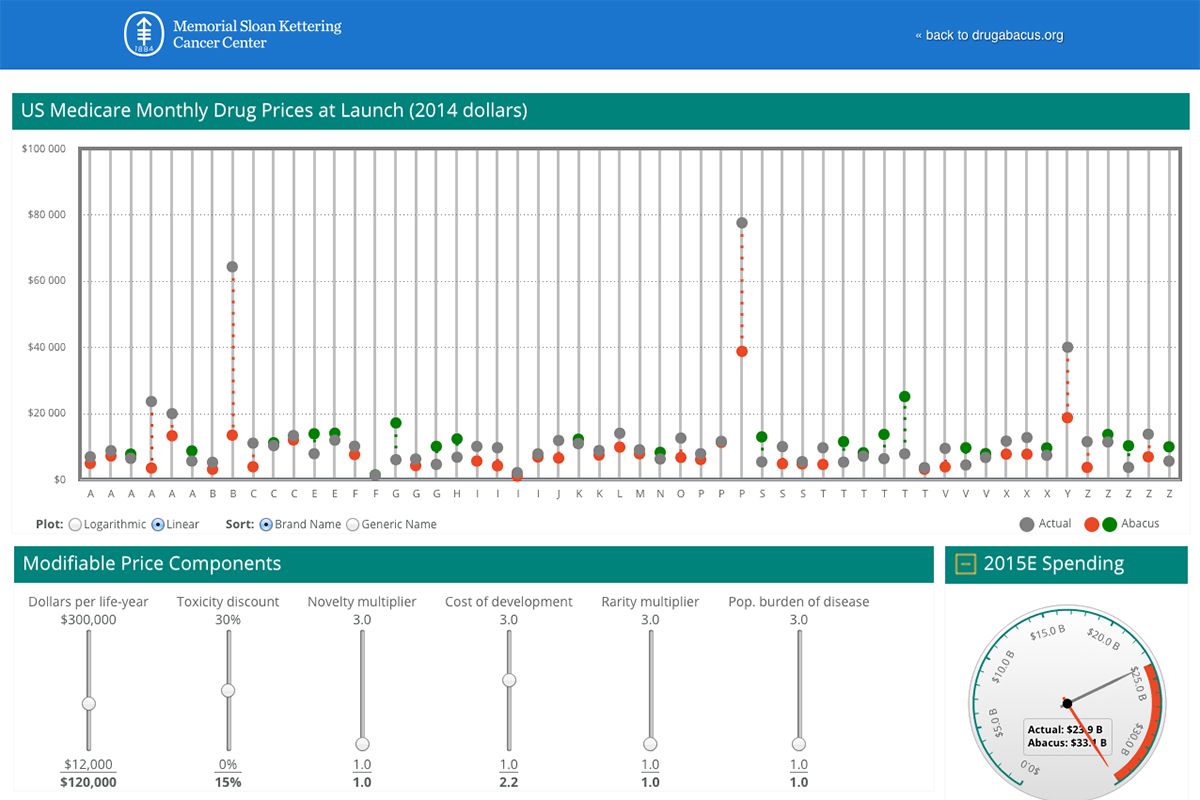
Yendo un paso más allá, ahora han diseñado una calculadora que permite estimar
el precio de más de 50 fármacos en función de su precio por año de vida
ganados, toxicidad, novedad, coste de desarrollo, frecuencia del cáncer y carga
de la enfermedad poblacional, y compararlo con su precio original.
Aunque esta calculadora ha sido comentada inluso en el Wall Street Journal, el hecho de que la iniciativa
surja de colectivos médicos diversos no hace más que mostrar su preocupación
por la sostenibilidad de la atención a este tipo de pacientes y las decisiones
difíciles a las que a menudo se enfrentan. Quizás estas iniciativas sirvan, si no
como palanca de cambio, sí como manera de empezar un debate social sobre qué y
cuanto estamos dispuestos a pagar.